Die Batteriefächer der 26S-Protein-Recyclinganlage
Der Abbau von Proteinen und die Wiederverwendung Ihrer Grundbausteine ist ein überlebenswichtiger Prozess in Zellen. Forscher am Max-Planck-Institut für Biochemie zeigen jetzt im Fachjournal PNAS die detaillierte Struktur der menschlichen Protein-Recyclinganlage, dem sogenannten 26S Proteasom, in fast atomarer Auflösung. Dies ermöglichte es den Wissenschaftlern unter anderem energieliefernde Moleküle am 26S Proteasom zu untersuchen, die notwendig sind, damit das Proteasom arbeitet. Das Wissen über den genauen Aufbau bietet die Grundlage zur Entwicklung von Medikamenten für die Krebstherapie und gegen neurodegenerative Krankheiten.
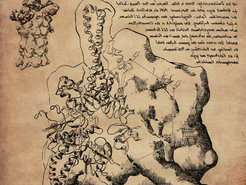
Zeichnung der Struktur des 26S Proteasoms, einem Teil der Protein-Recyclinganlage der menschlichen Zellen, im Stil von da Vinci. Die Skizze oben links zeigt den gesamten Komplex. Darunter ist der Teil mit den ‚Batteriefächern‘ (Bindestellen für ATP und ADP) im Detail gezeichnet.
Der Visionär, Leonardo da Vinci, konstruierte vor 500 Jahren komplexe Maschinen, wie Hubschrauber, die aus unserem heutigen Leben nicht mehr wegzudenken sind. Dafür zeichnete er detaillierte Baupläne. Heute versuchen Strukturbiologen die Baupläne von Proteinen, den molekularen Maschinen unserer Zellen, möglichst hoch auflösend zu rekonstruieren um ihre genaue Funktion zu verstehen. Allerdings sind die molekularen Maschinen etwa 100 Millionen Mal kleiner als die von da Vinci. Dies erfordert spezielle Methoden um sie sichtbar zu machen.
Wissenschaftler um Prof. Wolfgang Baumeister und Friedrich Förster zeigen jetzt den detaillierten, dreidimensionalen Aufbau des 26S Proteasoms in fast atomarer Auflösung. Die hochaufgelöste Struktur des 26S Proteasoms liefert vielfältige Erkenntnisse darüber, wie die einzelnen Teile der Maschine miteinander verbunden sind und zusammen arbeiten. Zur Aufklärung der Struktur nutzten die Wissenschaftler die Kryo-Elektronenmikroskopie.
Bei dieser Methode werden die Proteine aus Zellen isoliert und in dünnen Wasserfilmen schockgefroren. Dadurch verharren die vielfach vorkommenden zellulären Maschinen in verschiedenen Orientierungen und auf den mit dem Elektronenmikroskop aufgenommenen Bildern sind die Proteine aus unterschiedlichen Winkeln zu sehen. Mit Hilfe des Computers kann daraus, ähnlich wie bei der Computertomographie, eine dreidimensionale Struktur berechnet werden.
Als ein besonderes Detail zeigt die Struktur erstmals energieliefernde Moleküle, Adenosinphosphate. „Diese Moleküle funktioniert in unseren Zellen wie Batterien. Ist eine Batterie geladen liegt ATP, Adenosintriphosphate, vor, ist sie entladen, liegt Adenosindiphosphate, ADP, vor“, erklärt Andreas Schweitzer, Erstautor der Studie. „Wir konnten jetzt sozusagen die Batteriefächer des Proteasoms genau untersuchen.“ Doch wofür braucht das Proteasom Energie? Beim Proteinrecycling werden die Proteine vom 26S Proteasom auseinandergebaut, also entfaltet. Für diesen mechanischen Prozess, wird die Energie benötigt.
Deshalb hat das Proteasom 6 Batteriefächer, die in einem Sechseck angeordnet sind. Bislang war nicht bekannt, wie viele der Batteriefächer gleichzeitig mit Batterien gefüllt sein müssen, damit ausreichende Energie zur Verfügung steht. Die Wissenschaftler konnten nun mit Hilfe der Struktur ein atomares Model bauen und zeigen, dass im ruhenden Zustand, also zu einem Zeitpunkt, an dem kein Protein abgebaut wird, alle 6 Fächer mit Batterien gefüllt sind. Dabei ist die Energie von mindestens einer der Batterien bereits verbraucht; hier liegt ADP vor, während die übrigen Fächer wahrscheinlich ‚aufgeladene’ ATP-Moleküle enthalten - deutlich mehr als bisher angenommen.
„Die bis jetzt höchstaufgelöste Struktur des 26S Proteasoms ermöglicht es, eine Vielzahl von neuen Hypothesen über seine Funktion aufzustellen, die die Forschung auf diesem Gebiet prägen wird. Auf lange Sicht ist davon auszugehen, dass die Struktur als Grundlage für die Entwicklung von Medikamenten gegen spezielle Krebsarten und neurodegenerative Krankheiten dienen wird“, blickt Prof. Wolfgang Baumeister in die Zukunft. [AA]
Originalpublikation:
A. Schweitzer, A. Aufderheide, T. Rudack, F. Beck, G. Pfeifer, J. M. Plitzko, E. Sakata, K. Schulten, F. Foerster, and W. Baumeister: Structure of the human 26S proteasome at a resolution of 3.9 Å, PNAS, Juni 2016












