Struktur des zellulären Müllsacks
Max‐Planck‐Wissenschaftler identifizieren den Aufbau eines wichtigen Entsorgungssystems der Zelle
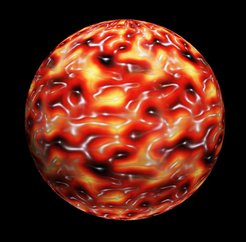
Das Bild zeigt die Struktur des Autophagozytose-Gerüstes. Mit Hilfe der atomaren Kraftmikroskopie konnte das Höhenprofil des Netzes auf der künstlichen Membran sichtbar gemacht werden. Von der Membran (schwarz) ausgehend erhebt sich allmählich (gelb-rot) das Netzwerk bis zum Höhengrad, der maximalen Dicke des Netzwerks (weiß). Diese zweidimensionale Karte wurde dann auf eine Kugel projiziert, die das Autophagosom darstellen soll.
Die Autophagozytose ist das Transportsystem der Zelle, welches den zellulären Abfall erkennt, verpackt, und zu zellulären Müllverbrennungsanlagen, den Lysosomen, transportiert. Somit dient die Autophagozytose vor allem dem Schutz der Zelle, indem sie verhindert, dass sich überschüssiges Material ansammelt. Ist die Autophagozytose verlangsamt oder vollständig gestoppt, können schwerwiegende Erkrankungen wie Alzheimer, Parkinson oder Krebs entstehen.
Ähnlich wie ein Müllsack den Abfall umschließt, legt sich während der Autophagozytose eine Membran um den zellulären Müll. Dieser molekulare „Müllsack“ wird als Autophagosom bezeichnet. Ist der Müll vollständig verpackt, transportiert die Zelle im nächsten Schritt das Autophagosom zu den Lysosomen, die ebenfalls von einer Membran umgeben sind. So kann der Abfall anschließend durch die Verschmelzung beider Membranen in das Innere des Lysosoms gelangen. Diese Organellen funktionieren wie Recyclinghöfe. Eine Vielzahl von Enzymen zerlegt darin das zu recycelnde Material in seine Grundbausteine.
Damit sich die Membran bei der Autophagozytose den unterschiedlichen Formen und Größen des Abfalls anpassen kann, muss sie vor allem flexibel sein. Zusätzlich benötigt sie jedoch ein mechanisches Gerüst, das den Müllsack stabilisiert. Thomas Wollert und seine Forschungsgruppe „Molekulare Membran- und Organell-Biologie“ konnten jetzt die molekulare Architektur dieses Stützgerüstes identifizieren und sichtbar machen.
Kleine Maschen – große Wirkung
Bei dem Gerüst handelt es sich um ein flaches Netz, das die Membran des Autophagosoms vollständig bedeckt. Die Knotenpunkte des Netzes bestehen aus einem kleinen Protein, Atg8, das als Membrananker dient und an die autophagosomale Membran geheftet wird. Ein weiterer Proteinkomplex vernetzt die membranverankerten Atg8-Moleküle miteinander und bildet so das Gerüst. Die Länge einer Masche beträgt nur 16 millionstel Millimeter (16 nm) und das Netz ist nur 8 millionstel Millimeter (8 nm) dick. Hat die Membran den Abfall vollständig umschlossen, wird das Gerüst wieder entfernt, indem ein Enzym Atg8 von der Membran schneidet.
Die Wissenschaftler waren zudem in der Lage, den Auf- und Abbau des Gerüstes an künstlichen Membranen im Reagenzglas nachzubilden und live zu verfolgen. „Es ist wichtig, dass wir diesen Prozess begreifen, um ihn gezielt steuern zu können“, beschreibt Thomas Wollert, Forschungsgruppenleiter am MPIB, seine Ergebnisse. „Könnten wir die Autophagozytose zum Beispiel beschleunigen, ließen sich zukünftig vielleicht Krankheiten wie Krebs oder Alzheimer heilen.“[VS]
Originalpublikation:
Kaufmann A., V. Beier, H. G. Franquelim and Wollert T., Molecular Mechanism of Autophagic Membrane-Scaffold Assembly and Disassembly, Cell, January 30, 2014.
DOI: 10.1016/j.cell.2013.12.022




