Durch das Fabriktor Sec61 in die Membran
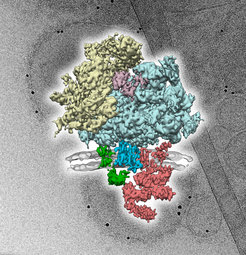
Eiweiße werden im Ribosom (beige, hellblau) aus Aminosäuren zusammengefügt. Danach werden sie durch den Kanal Sec61 (blau) geleitet und in die Membran (grau) eingebaut. Weitere Komponenten (grün, rot) sind an der Modifikation und Faltung neu hergestellter Eiweiße beteiligt. Der dreidimensionale Eiweißkomplex (Vordergrund) wurde aus vielen zweidimensionalen Bildern rekonstruiert (Hintergrund), die am Kryo-Elektronenmikroskop aufgenommen wurden.
Eiweißmaschinen bestehen aus langen, verschlungenen Aminosäureketten. Das Zusammenfügen dieser Aminosäuren zu den Eiweißen findet im Ribosom statt. Nach ihrem Zusammenbau wird ungefähr ein Drittel aller Eiweiße in zelluläre Membranen eingebaut, wo sie dann zum Beispiel als Kanal oder Rezeptor arbeiten.
Nicht nur der Aufbau der Eiweiße, sondern auch ihr Einbau in eine Membran, stellt eine große Herausforderung dar. In allen Zellen ist der Kanal Sec61 für diese Aufgabe zuständig. Genau wie die Eiweiße, die durch den Sec61-Kanal geleitet werden, ist auch Sec61 in eine Membran eingebaut: Eine Maschine, die bei der Herstellung von Maschinen hilft. Aufgrund seiner zentralen Aufgabe ist Sec61 für das allgemeine Verständnis von Zellfunktionen von zentraler Bedeutung, aber auch für das Verständnis von Krankheiten. So war der genaue Aufbau von Sec61 bereits Ziel mehrerer Studien. „In allen bisherigen Studien wurde der Kanal jedoch aus seiner natürlichen Membranumgebung herausgelöst", berichtet Friedrich Förster, Leiter der Forschungsgruppe „Modellierung von Proteinkomplexen“. "Wir wollten wissen, ob dadurch die Struktur und Funktion von Sec61 verändert wird."
Seine Arbeitsgruppe untersuchte Sec61 mit Hilfe der Kryo-Elektronentomographie. Dabei nutzten sie ein neues, hochauflösendes Direktdetektorsystem, mit dem sie den Aufbau von Sec61 in seiner natürlichen Membranumgebung in nicht dagewesener Auflösung untersuchen können. Hierzu wird die Probe zunächst „schockgefroren“, damit sie ihre Form behält. Dann nehmen die Forscher aus verschiedenen Blickwinkeln zweidimensionale Bilder des Objekts im Elektronenmikroskop auf. Im Anschluss werden diese Bilder zu einem dreidimensionalen Bild rekonstruiert. „In ähnlicher Weise funktioniert ein Computertomograph in der Medizin“, sagt Friedrich Förster. Mit dieser Methodik können jetzt natürliche Strukturen mit einer Auflösung von weniger als 1nm untersucht werden. Dies ermöglicht Rückschlüsse fast bis auf die Ebene der Aminosäuren. „Erstaunlicherweise scheint sich Sec61 in seiner natürlichen Membranumgebung anders zu verhalten, als im isolierten Zustand. Das verändert unsere Vorstellung vom Prozess, wie Eiweiße in die Membran eingebaut werden wesentlich“, fasst Förster die Ergebnisse der aktuellen Studie zusammen.
Originalpublikation:
Pfeffer, S., Burbaum, L., Unverdorben, P., Pech, M., Chen, Y., Zimmermann, R., Beckmann, R., Förster, F.: Structure of the native Sec61 protein-conducting channel. Nature Communincations, September 28, 2015
Doi:10.1038/ncomms9403 (2015).



