Wie menschliche transfer-RNAs hergestellt werden
Forschende unter der Leitung von Danny Nedialkova am MPI für Biochemie entdeckten die Mechanismen zur Regulierung der tRNA-Expression in menschlichen Zellen, die die gezielte Weiterentwicklung tRNA-basierter Medikamente ermöglichen.
Der menschliche Körper besteht aus Tausenden verschiedenen Zelltypen, die wiederum einzigartige Sätze an Proteinen enthalten. Die Herstellung dieser Proteine hängt von den transfer-RNAs (tRNAs) ab, die die Aminosäuren an die Ribosomen liefern, den Ort der Proteinherstellung. Kommt es in diesem Prozess zu Fehlern, können nicht funktionierende Proteine und neurologische Erkrankungen die Folge sein. Forschende um Danny Nedialkova am Max-Planck-Institut (MPI) für Biochemie haben nun die Mechanismen entdeckt, die dafür verantwortlich sind wie verschiedene Zelltypen ihre tRNA-Zusammensetzung im Laufe ihrer Entwicklung beibehalten. Die Studie wurde in der Fachzeitschrift Nature Cell Biology veröffentlicht.
Um die Proteine herstellen zu können, die für das Wohlergehen unserer Zellen und damit auch für unsere Gesundheit entscheidend sind, muss die in unserer DNA gespeicherte Information entschlüsselt und übersetzt werden. Dazu wird unsere DNA zunächst in kürzere Stränge, die so genannte Boten-RNA (mRNA), umgeschrieben werden. Obwohl jede Zelle in unserem Körper dieselbe genetische Information enthält, werden in den verschiedenen Zelltypen unterschiedliche Teile dieser Information genutzt. Die Regulierung welche Teile verwendet werden stellt sicher, dass während des gesamten Lebens einer Zelle nur die wirklich notwendigen Proteine hergestellt werden. Die produzierten mRNA-Baupläne werden dann von Ribosomen abgelesen und mit Hilfe von tRNAs, kurzen RNA-Molekülen mit kleeblattartiger Struktur, zu Proteinen zusammengesetzt. Jede tRNA trägt eine der zwanzig Aminosäuren, die als Bausteine dienen, und bindet an ein spezifisches Codon auf der mRNA.
Es gibt 61 Codons für alle zwanzig Aminosäuren, aber die Anzahl der tRNA-Moleküle die sie entschlüsseln unterscheidet sich je nach Organismus und Zelltyp erheblich. Daher ist es eine Herausforderung zu bestimmen, wie genau die Anzahl in menschlichen Zellen reguliert wird, denn im menschlichen Genom gibt es mehr als 600 Gene die für tRNAs kodieren, von denen viele an mehreren Stellen zu finden sind.
Darüber hinaus ist die tRNA-Expression bei Säugetieren extrem komplex, aber bisher ist noch nicht bekannt, wie sie genau funktioniert. Die Bestimmung dieser Mechanismen, die die tRNA-Häufigkeit kontrollieren ist von entscheidender Bedeutung um zu verstehen, wie tRNA-Defekte beispielsweise zu neurologischen Erkrankungen führen.
Die Vermessung der (tRNA) Welt in menschlichen Zellen
Die Struktur und die zahlreichen chemischen Modifikationen der tRNAs machen es schwierig, ihre Menge in Zellen mit herkömmlichen Techniken zu messen. Das Team von Danny Nedialkova hat diese technologische Barriere kürzlich durch die Entwicklung einer Methode namens mim-tRNAseq überwunden, die tRNAs mit zuvor unerreichter Genauigkeit und Auflösung misst. Dadurch fand das Team heraus, dass die Anzahl der Genkopien in menschlichen Zellen kein sehr guter Indikator für die Häufigkeit der tRNAs ist. Das wirft wiederum die Frage auf, wie menschliche tRNA-Repertoires kontrolliert werden und wie stark sie zwischen verschiedenen Zelltypen variieren.
Nicht alle menschlichen tRNA-Gene sind gleich
„Es gibt die Theorie, dass die tRNA-Pools auf das einzigartige Proteom jedes Zelltyps zugeschnitten sind“, erklärt Danny Nedialkova, Max-Planck-Forschungsgruppenleiterin am MPI für Biochemie und Professorin an der Fakultät für Biowissenschaften der Technischen Universität München. „Da Herzzellen viele Sarkomerproteine synthetisieren, benötigen sie vielleicht größere Mengen spezifischer tRNAs, die beispielsweise in Gehirnzellen nicht so sehr benötigt werden. Das ist dann ein bisschen wie in einer Küche, in der man in einem Sushi-Restaurant mehr Lachs braucht als in einer Bäckerei“, so Nedialkova weiter.
Um diese Theorie zu testen, entwickelte Lexi Gao, Co-Erstautorin der Studie, einen Arbeitsablauf zur Spezialisierung menschlicher induzierter pluripotenter Stammzellen in Gehirnzellen oder Herzzellen im Labor. Dadurch war es den Forschenden möglich, die tRNA-Regulation direkt in physiologisch relevanten Zellmodellen zu untersuchen. „Wir waren überrascht, dass trotz der erheblichen Umgestaltung des tRNA-Repertoires während der Differenzierung die Häufigkeit von tRNAs, die zu jedem mRNA-Codon passen, bei allen Zelltypen nahezu identisch war und auch die Verwendung der verschiedenen mRNA-Codons stabil blieb“, sagt Lexi Gao.
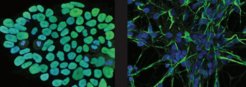
Gemeinsam mit Co-Erstautor Andrew Behrens zeigte Lexi Gao, dass einzelne tRNA-Gene sehr ungleich ausgeprägt sind. „Nur etwa ein Drittel der menschlichen tRNA-Gene wurde in allen Zelltypen nachgewiesen. Diese Gene - die wir als ‚Housekeeping‘-Gene bezeichnen - haben bestimmte Sequenzen, die die Rekrutierung der RNA-Polymerase III für die Transkription begünstigen. Aus den Housekeeping-tRNA-Genen entstanden auch die in den meisten Zelltypen am häufigsten vorkommenden tRNAs“, erklärt Behrens.
Die Stabilität von tRNA-Pools, die bei verschiedenen Zelltypen zu unterschiedlichen Codons passen, könnte das Potenzial für Übersetzungsfehler an Ribosomen während der Entwicklung minimieren. „Eine universelle Restaurantküche hat vermutlich auch ihre Vorteile. Es nützt schließlich nichts, einen Kühlschrank voller Lachs zu haben, wenn man einen Schokoladenkuchen backen will“, so Nedialkova.
Von Vorhersagen in die Therapie
Die von Nedialkovas Team ermittelten Regeln für die tRNA-Expression haben wichtige Auswirkungen auf das neu entstehende Feld der tRNA-Medizin. Die Entwicklung von Suppressor-tRNAs, die vorzeitige Abbruchcodons in der mRNA umgehen können, könnte eine Behandlung für Tausende von menschlichen Erbkrankheiten bieten.
Bisher konzentrierte sich das Design von Suppressor-tRNAs vor allem auf die Identifizierung von Molekülen, die in den Zellen mit Aminosäuren beladen werden können und die das Überlesen natürlicher STOP-Codons nicht auslösen. „Unsere Daten zeigen, dass die Wirksamkeit von Suppressor-tRNA-Therapeutika auch stark von der Wahl der Sequenzelemente abhängt, die die Transkription der RNA-Polymerase III regulieren", sagt Danny Nedialkova abschließend.
[tb]
Wörterbuch der Forschungsgruppe Mechanismen der Proteinbiogenese
mRNA: Boten-RNA-Moleküle, die den Bauplan für Proteine an das Ribosom liefern.
Ribosom: Die proteinbildende Maschinerie in Zellen, die den mRNA-Sequenzplan in die entsprechenden Aminosäuren übersetzt, um ein neues Protein zusammenzusetzen.
tRNA: Transfer-RNA, kurze Moleküle, die während der Übersetzung der Boten-RNA in Proteine spezifische Aminosäuren an die Ribosomen liefern
mim-tRNAseq: eine vom Team um Danny Nedialkova entwickelte Methode zur genauen Messung der Menge jeder tRNA in Zellen. Weitere Informationen finden Sie hier.
Humane induzierte pluripotente Stammzellen: sich selbst erneuernde Zellen, die durch Umprogrammierung menschlicher Haut- oder Blutzellen gewonnen werden, um deren Fähigkeit zur Differenzierung in nahezu jede Art von Zelle im Körper wiederherzustellen.
Polymerase: ein Enzym, das DNA- oder RNA-Moleküle aus ihren Grundbausteinen in Zellen zusammensetzt.



